時間をコントロールして病気を治す
Drug Discovery Study for Time Medicine
時間を基軸にこれまでの病気の概念や創薬のあり方を変える。システムバイオロジー分野では生体リズムを基盤とした時間医薬科学の創成を目指しています。体内時計の時刻や振幅をコントロールできるようになれば、従来の対処法とは異なる新たな時間治療が実現できると私たちは考えています。不眠症に代表される生体リズム障害や、これまで原因の不明だった高血圧症や加齢性のさまざまに疾患に対し、早期の予防や新規の診断分類法が確立され、従来にはない新しい作用の時間治療薬が開発されると期待しています。
研究課題の紹介

加齢性臓器連関障害の原因となる脳内サーカディアンリズム中枢の役割、および、加齢性臓器機能障害における末梢時計の役割を現在研究しています。体内時計を活用した抗老化・健康維持プロトコルの作成を行うとともに、体内時計を介した老化機構の本質へ迫りたいと考えています。
See: Sasaki et al Nature Aging, 2022; Hamada et al Ocul Surf, 2022

我々は、生体リズムの中枢を調整するオーファンG蛋白質共役受容体Gpr176を同定しました。G蛋白質共役受容体は薬理学上最も重要でかつ効率のよいターゲットとして知られる分子群です。現在、化合物ライブラリーの網羅探索による生体リズム調整薬の開発を目指しています。
See: Doi et al Nature Commun, 2016; Wang et al Sci Rep, 2020; Yamaguchi et al Sci Rep, 2021
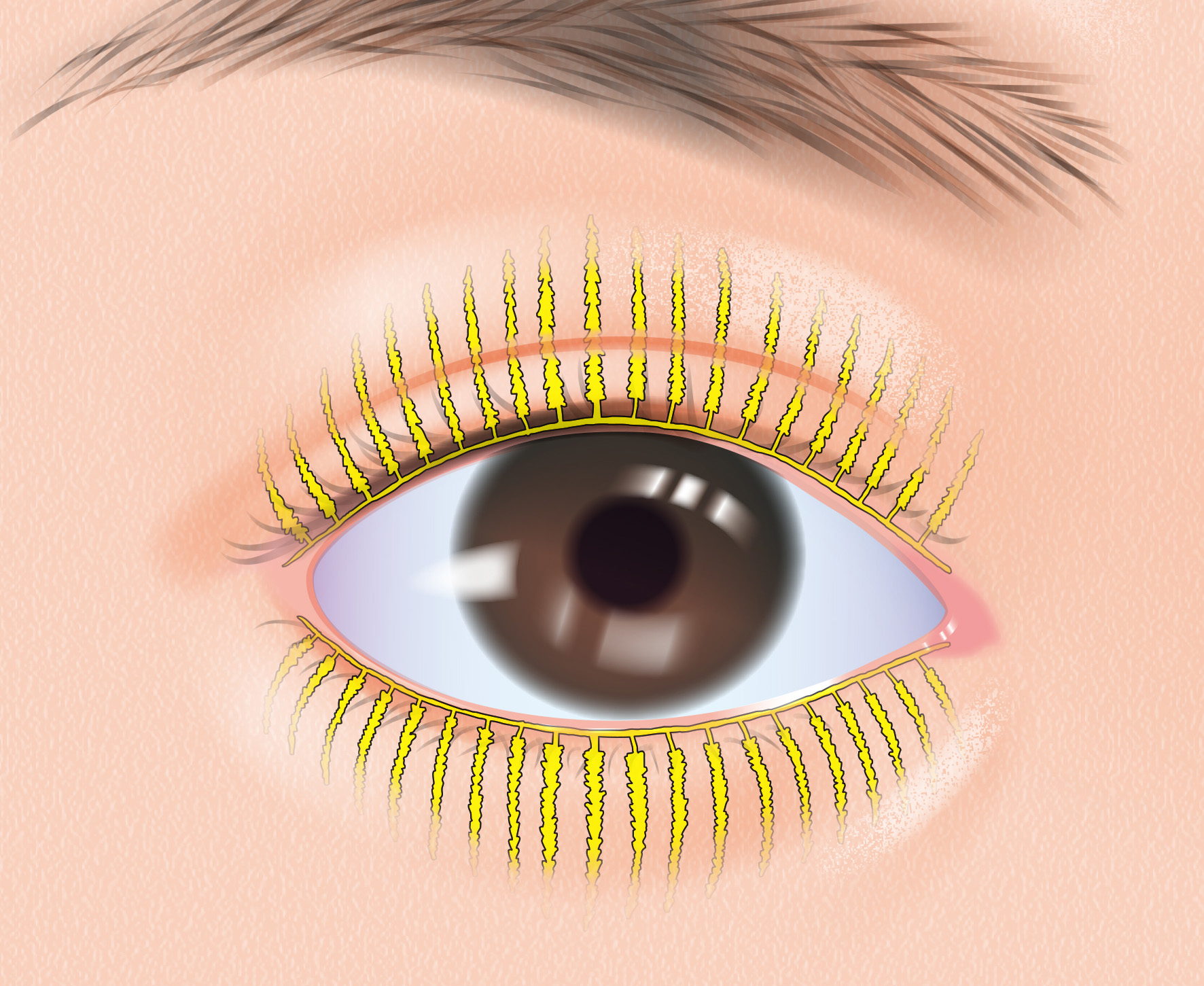
まぶたにあるマイボーム腺は、眼の乾燥を防ぐため眼表面にマイバムを産出します。アンドロゲンはこのなかで作られ、組織の維持に必要ですが、臨床応用には課題がありました。局所的な代謝物への変換/不活性化が隠されているためです。我々はヒトにおいて、アンドロスタンジオン、アンドロステロン、エピアンドロステロンがその代謝物であることを示しました。これら代謝物マーカーは、マイバムを利用した眼の機能評価に役立つと期待されます。See: Nguyen Pham et al iScience, 2025

生命活動を司る「脳」をより深く理解するためには、その活動を観察・評価するだけでなく、脳の働きを意図的に操作してその結果を調べることが重要です。我々は、G蛋白質共役受容体を独自に改良し、神経活動を精度よく上下(正負)にコントロールできる技術を開発しました。これを脳波と組み合わせて、睡眠・眠気や脳の覚醒スイッチの謎に迫ります。
See: Miyake et al Cell Rep Methods, 2024

時計遺伝子そのものではなく時計遺伝子の発現を制御するDNA配列が、動物の体温や活動の24時間リズムをコントロールするスイッチになっていることを示しました。タンパク質をコードしないDNAスイッチの発見は、人間の朝型・夜型、睡眠パターンの違いを解明する手がかりになるかもしれないと考えています。
See: Doi & Shimatani et al Nature Commun, 2019; Tainaka et al Chronobiol Int, 2018
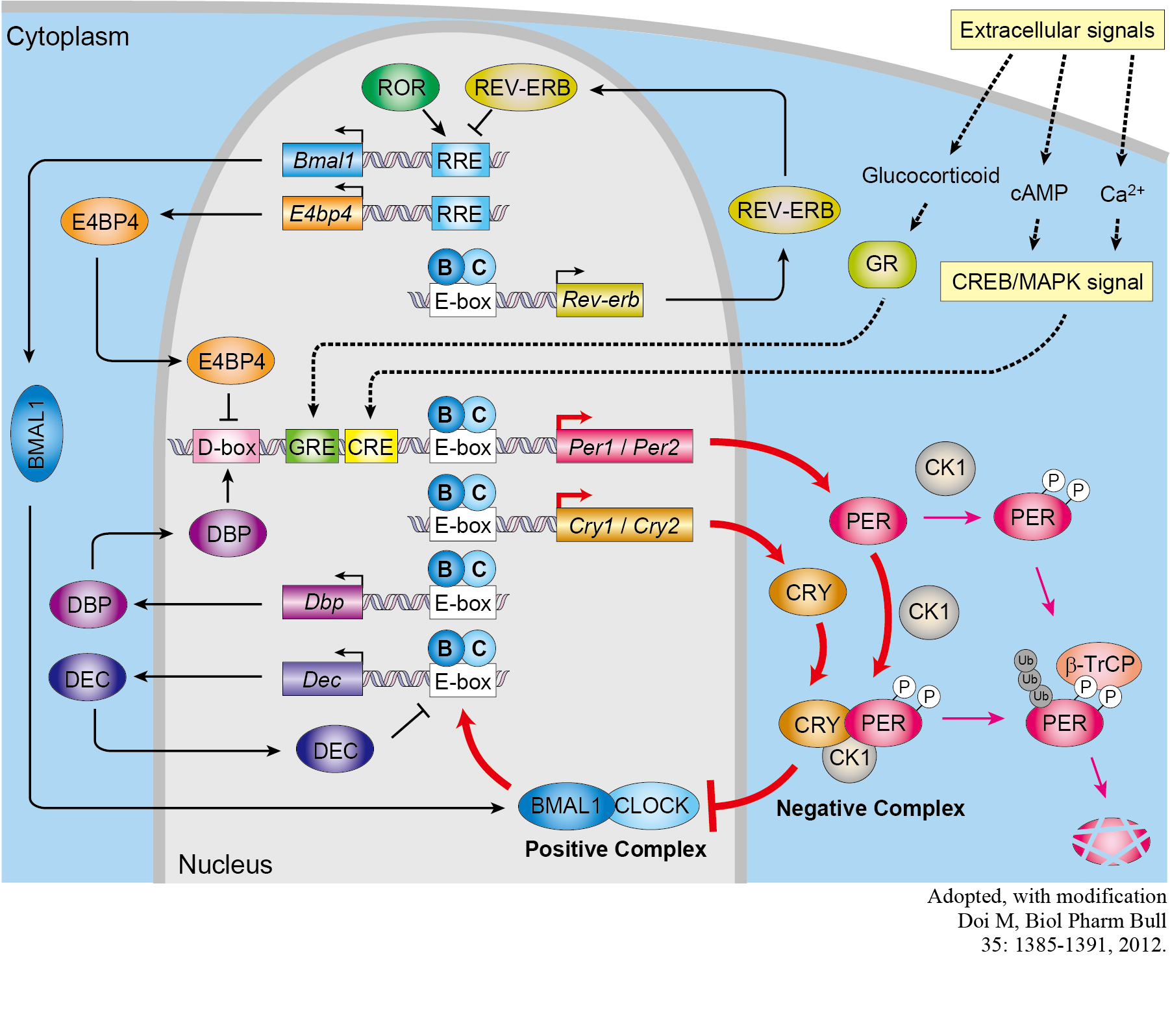
生体リズムの研究分野は、24時間周期の体内リズムが時計遺伝子の自己制御型フィードバックによって生み出されるという発見を契機に発展し、今やノーベル賞を受賞するに至りました。 しかし、今なお生物時計の制御には説明できない事象が数多くあり、蛋白質やmRNAの化学修飾をはじめとした転写によらない時計機構に、近年ようやく光が当たりはじめています。
See: Doi et al PNAS, 2001; Doi et al Curr Biol, 2004; Doi et al Cell, 2006; Doi et al Nature Neurosci, 2006; Fustin et al Cell, 2013

目覚まし蛋白質RGS16を同定しました。RGS16はGpr176の下流に位置するG蛋白質制御因子です。ヒトの大規模コホート研究からも「朝型」を規定する遺伝子だと分かり、我々の研究の有効性がヒトでも確認されています。朝型 vs. 夜型の分子機構をさらに掘り下げて創薬につなげたいと考えています。
See: Doi et al Nature Commun, 2011
Cf. Jones et al Nature Commun, 2019

昼寝の体温を制御するG蛋白質共役受容体を発見しました。この受容体は脳内のサーカディアンリズム中枢に発現し、体温の日内変動を制御します。昼寝の生物学的意義についてはまだまだ不明な点が多く、今回の知見を突破口にしてその謎へ迫りたいと考えています。
See: Goda & Doi et al Genes Dev, 2018
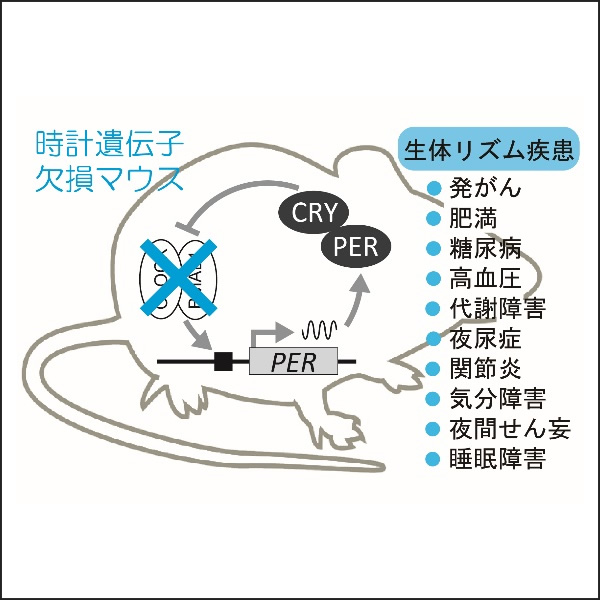
私たちは、高血圧の他にも、関節リウマチ、夜間頻尿、エネルギー代謝障害や肝臓細胞の多倍体化に体内時計が関与することを示しました。こうした研究から、現在、生体リズムの異常は、現代社会にみられる多くの生活習慣病の根底に潜む共通の病因の1つであると認識されています。
See: Chao et al Nature Commun, 2017
2010年、私たちは、体内時計の異常が食塩感受性高血圧につながることを示しました。食塩を採りすぎると血圧が上がる、という、誰もが知る「コモンディジーズ」のうら側に体内時計の異常が一因としてある、ということを示しました。
See: Doi et al Nature Med, 2010

我々の体のリズムを生み出す時計のセンターは脳の奥底にあり、そこでは数千個のニューロンが特有のパターンで振動を生み出しています。ニューロンによる「同期」と「演算」が体内時計の頑強さと外部環境への柔軟な適応性を生み出しているのです。我々は体内リズムを支配する脳内の神経回路ネットワークを解明しようと研究を進めています。
See: Doi et al Nature Commun, 2011; Yamaguchi et al Science, 2013

大学の研究はベンチで行う基礎研究がすべてではありません。ベンチで得た知見をベッドサイドへ届けることが薬学人の夢であり、橋渡し研究は重要な課題です。我々は生体リズム異常マウスで見つけた高血圧症の原因分子をうまく利用してヒトの治療に役立てようと努力しています。既にヒト臨床診断用モノクロ抗体の作製に成功し特許を取得しました。
See: Doi et al JCEM, 2014; Ota et al MCB, 2014; Yamamura et al MCE, 2014